Über- und Unterdrainage
- die häufigsten "Nebenwirkungen" eines Shuntsystems
Ein Blick zurück auf 70 Jahre Shunt-Historie mit Über- und Unterdrainage
Über- und Unterdrainage sind auf das Engste mit der normalen physikalischen Funktion des Shunts verbunden. Es handelt sich hierbei nicht um eine z.B. durch Unachtsamkeit oder Unverständnis herbeigeführte „Fehlfunktion“, sondern vielmehr um eine zwangsläufige Folge der künstlichen, unphysiologischen Verbindung zwischen normalerweise getrennten Körperhöhlen durch den Shunt. Deshalb ist es so wichtig die physikalischen Grundlagen beider Phänomene zu kennen, um ihnen mit der richtigen Kombination aus Therapie und Technologie entgegen wirken zu können.
mehr lesen„Ein Shunt ist wie ein Pferd, das vor ein Auto mit Motordefekt gespannt wird.“
Der Hydrocephalus hat viele verschiedene Erscheinungsformen und Ursachen. Obwohl das Krankheitsbild schon seit der Antike bekannt ist, sind die meisten dieser Ursachen „nicht besonders gut verstanden“, wie man in der Wissenschaft sagt - oder sogar gänzlich unbekannt. Und Ursachen, die man nicht kennt oder nicht versteht, kann man auch nur schwer bekämpfen. Dabei ist diese Erkrankung gar nicht so selten und kann jede Altersgruppe treffen.
Bis auf den heutigen Tag werden nur die Symptome behandelt, indem der für die Patienten gefährliche Überdruck im Schädel mittels eines Ventils reduziert und in eine andere geeignete Körperhöhle (z.B. häufig den Bauchraum) abgeleitet wird.
SHUNTSYSTEM
Ein Shuntsystem besteht üblicherweise mindestens aus einem Ventrikelkatheter (proximal), einem Ventil (frontal oder occipital) zur Regelung des Öffnungsdruckes und einem (distalen) Katheter für die Ableitung in eine bestimmte Körperhöhle (rechter Herzvorhof oder Bauchraum). Zusätzlich kann so ein Shuntsystem mit einem Reservoir (Bohrlochreservoir oder Vorkammer) ausgestattet sein.
Der erste Shunt wurde vor fast genau 70 Jahren (d.h. 1949) von den beiden Neurochirurgen Spitz und Nulsen in Philadelphia implantiert. Er war so primitiv und fehleranfällig, dass er - soweit bekannt - nur einem einzigen Patienten für kurze Zeit half. Sechs Jahre später wurde das Ventil ganz entscheidend von dem Schlosser John Holter verbessert, so dass man die „Ära der Shunt-Therapie“ meistens erst ab 1955 beginnen lässt. Die berühmte Geschichte, wie John Holter verzweifelt (und leider am Ende doch vergeblich) um das Leben seines neugeborenen, an Hydrocephalus erkrankten Sohnes kämpft, ist auf dieser Webseite besonders eindrücklich beschrieben: HOLTER'S BRAIN DRAIN.
Seitdem ist das Grundprinzip des „Shuntings“ unverändert geblieben: So etwas ist ungewöhnlich im Bereich der Medizin. Rein technisch gesehen hat sich allerdings Vieles deutlich verbessert. Gute Shunts sind heute aus biokompatiblen und widerstandsfähigen Materialien, so dass sie weder brechen, noch korrodieren oder Abstoßungs-Reaktionen hervorrufen. Die Infektionsraten können mit antibakteriellen Kathetern unter 5% gedrückt werden (Ritz1, 2007; Parker2, 2015) und die Öffnungsdrücke sind individuell an die Bedürfnisse des Patienten anpassbar. Viele der Patienten können mit solchen modernen Shunts über lange Zeiträume ein fast unbeeinträchtigtes Leben führen und das ist in der Tat ein großer Fortschritt.
Dennoch führt das immer noch geringe Wissen über die Ursachen eines Hydrocephalus trotz guter, moderner Shunts zu Problemen bei der Behandlung der Erkrankung.
Vielleicht ist es ein hilfreiches Bild, den Shunt mit einem Pferd zu vergleichen, das vor ein Auto mit Motordefekt gespannt wird. Obwohl über die Ursache des Motorschadens nichts Genaues bekannt ist, bewegt sich das Auto wieder (… wenn auch etwas langsamer …) und kann durchaus das ursprünglich geplante Ziel erreichen. Ob eine gerissene Benzinleitung, ein geplatzter Motorblock oder eine defekte Zündkerze ursächlich waren, ist dabei ganz egal, denn die Methode funktioniert erst einmal fast immer. Man muss nur ein paar neue Regeln einhalten: z.B. dem Pferd regelmäßig Futter geben oder Ruhezeiten für das Pferd einhalten. UND: Es können nun plötzlich ganz neue, andere Dinge schief gehen. Das Pferd kann auf holperiger Piste einfach los galoppieren und das Auto in eine falsche Richtung oder sogar in den Graben ziehen. Der Fahrer, der vorher nur sein Auto kennen musste, muss nun auch das Pferd antreiben können und verstehen lernen.
Ein Shunt kann z.B. mit der Zeit verstopfen und bis heute kann man selten mehr dagegen tun, als einen neuen zu implantieren. Ein anderer, besonders unangenehmer, aber unvermeidbarer Nebeneffekt ist das sogenannte „Siphoning“: Aufgrund der physikalischen Gesetze ergibt sich in stehender Position zwischen Kopf und Bauchraum ein hoher Sog (oder negativer Druck) in den Ventrikeln, weil die Flüssigkeit im Katheter durch die Gravitation nach unten gezogen wird. Dieser Sog ist für das Gehirn genau so gefährlich wie der ursprüngliche Überdruck (Hydrocephalus), denn es können z.B. Hirn-Blutungen dadurch hervorgerufen werden. (Ausführliche Informationen zu diesem Phänomen bietet dieser Artikel: "Grundkurs Fluidmechanik oder von Bechern, Flaschen und Menschen?")
Dieser Nebeneffekt kann durch einen normalen Shunt nicht abgefangen werden: es bedarf spezieller Techniken, um ihn zu kompensieren.
Die Unterdrainage, aber mehr noch die besonders gefährliche Überdrainage sind daher auf das Engste mit der normalen physikalischen Funktion des Shunts verbunden. Es handelt sich hierbei nicht um eine z.B. durch Unachtsamkeit oder Unverständnis herbeigeführte „Fehlfunktion“, sondern vielmehr um eine zwangsläufige Folge der künstlichen, unphysiologischen Verbindung zwischen normalerweise getrennten Körperhöhlen durch den Shunt.
Bei der heute nach wie vor häufigen Implantation eines einzelnen verstellbaren Differenzdruckventiles ist entweder eine Überdrainage oder eine Unterdrainage praktisch unvermeidbar und der behandelnde Arzt kann nur durch geschickte Einstellung des Ventils einen unter Umständen „klinisch-akzeptablen“ Kompromiss zwischen beiden herbeiführen. Wirklich zu vermeiden ist insbesondere die Überdrainage und ihre mitunter dramatischen Folgen für den Patienten nur durch die zusätzliche Implantation eines Ventils, das in der Lage ist, diesen physikalischen Kräften entgegen zu wirken, wie im Folgenden gezeigt werden soll.
Unterdrainage bedeutet, dass zu wenig Liquor durch den Shunt abgeführt wird. Der pathologische Überdruck in den Ventrikeln kehrt quasi zurück oder wird nur unzureichend abgebaut. Die ursprünglichen Symptome des Hydrocephalus treten dann teilweise oder vollständig erneut auf: Kopfschmerzen, Schwindel und Übelkeit. Bei Kindern treten ggf. zusätzlich eine Veränderung des Blickes (Sonnenuntergangsphänomen, Stauungspapille) und ein langsames Anwachsen des Kopfumfanges auf. Bei NPH-Patienten sind die Leit-Symptome Inkontinenz, demenzartige Verwirrung und die typische kleinschrittige Gangstörung. Diese äußerlich sichtbaren Symptome sind dabei permanent: vor allem treten sie unabhängig davon auf, ob der Patient steht oder liegt.

Im MRT- oder CT-Bild zeigt sich unter Umständen, dass der Überdruck bei der Unterdrainage dazu führt, dass sich die Ventrikel weiten und das Hirngewebe komprimiert und von innen gegen die Schädelwand gedrückt wird. Dabei werden Nervenzellen zerstört und sterben ab. Dieser Prozess vollzieht sich in Abhängigkeit von der Höhe des Überdruckes zwar langsam über Wochen und Monate, aber er ist auf Dauer irreversibel, da sich Nervenzellen nicht regenerieren.
Die Unterdrainage ist ohne Weiteres dadurch erklärbar, dass das Ventil einen zu großen Durchflusswiderstand und/oder einen zu hohen Öffnungsdruck hat: es erfüllt einfach nicht ausreichend seine vorgesehene therapeutische Funktion. Ist in so einem Fall ein verstellbares Ventil implantiert, muss daher als erste Gegenmaßnahme der Öffnungsdruck heruntergestellt werden, um das Ventil schon bei einem geringeren Überdruck zu öffnen und somit ein früheres Abfließen von Hirnwasser zu ermöglichen. Führt dies zu keiner Besserung, könnte eine Verstopfung des Ventils vorliegen und eine Revision ist dann unvermeidlich.
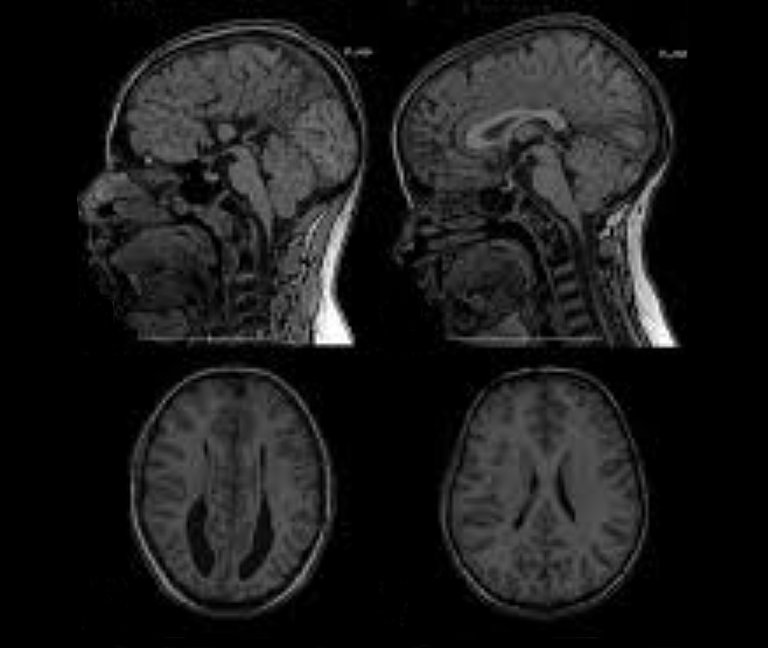
Überdrainage bedeutet, dass zu viel Liquor abgeführt wird und ein zu niedriger intraventrikulärer Druck, teilweise sogar ein Sog in den Ventrikeln besteht.
Die äußerlich sichtbaren akuten Symptome sind weitgehend dieselben wie bei der Unterdrainage, nämlich Kopfschmerzen, Schwindel und Übelkeit. Beide Komplikationen sind daher zunächst kaum voneinander zu unterschieden.
In der Bildgebung kann sich bei einer Überdrainage allerdings zeigen, dass die Ventrikel im Unterschied zur Unterdrainage geschrumpft oder sogar ganz in sich zusammengefallen sind – sie werden dann als Schlitzventrikel bezeichnet.
Schlitzventrikel für sich genommen haben zunächst keinen Krankheitswert. Der Begriff bezeichnet nur die Weite der Hirnwasserkammern, die infolge von Überdrainage schlitzförmig verengt sind. Ein solches Erscheinungsbild der Ventrikel im CT oder MRT bestätigt aber z.B. die Verdachtsdiagnose "Überdrainage".
INTRAVENTRIKULÄRER DRUCK
Der intraventrikuläre Druck (engl: Intraventricular Pressure = IVP) ist ein Differenzdruck bezogen auf den äußeren Atmosphärendruck. Ein „negativer IVP“ oder Sog liegt also dann vor, wenn der Druck in den Ventrikeln kleiner als der Luftdruck ist.
Infolge von Überdrainage wird das Hirngewebe unter eine erhebliche Spannung gesetzt, allerdings nicht durch Kompression, sondern durch eine Zug- oder Dehnungsspannung, die die Kortex-Oberfläche von der Schädelwand in Richtung Ventrikel wegzieht. Es gibt sogar dokumentierte Fälle, in denen der ganze Hirnstamm oder das Kleinhirn durch diesen Sog räumlich verschoben werden und das äußerst dünne Aquädukt (der wichtige Verbindungskanal zwischen III. und IV. Ventrikel) dabei abgeknickt wird.
Die bildgebenden Verfahren führen aber nicht immer und auch nicht sofort zu derart eindeutigen Diagnosen, sondern sind häufig unauffällig: die genannte morphologische Veränderung der Ventrikel und des Hirns benötigen einige Zeit und hängen natürlich auch von der Stärke der Überdrainage und der Compliance des Gehirns ab.
Compliance
Ein besonders wichtiger Begriff im Bereich der Hydrocephalus-Therapie ist die sogenannte „Compliance“. Sie charakterisiert nicht nur das Gehirn, sondern das gesamte Zentrale Nervensystem (ZNS), d.h. den Schädelinnenraum und den Rückenmarkskanal. Diese Räume sind überwiegend mit Hirngewebe und Rückenmark gefüllt (ca. 1400 ml) , ebenso mit arteriellem und venösem Blut (zusammen ca. 150 ml, im Verhältnis 1:2) sowie mit CSF (englisch: Cerebrospinal fluid = CSF oder auch „Liquor“ genannt: ca. 150 ml).
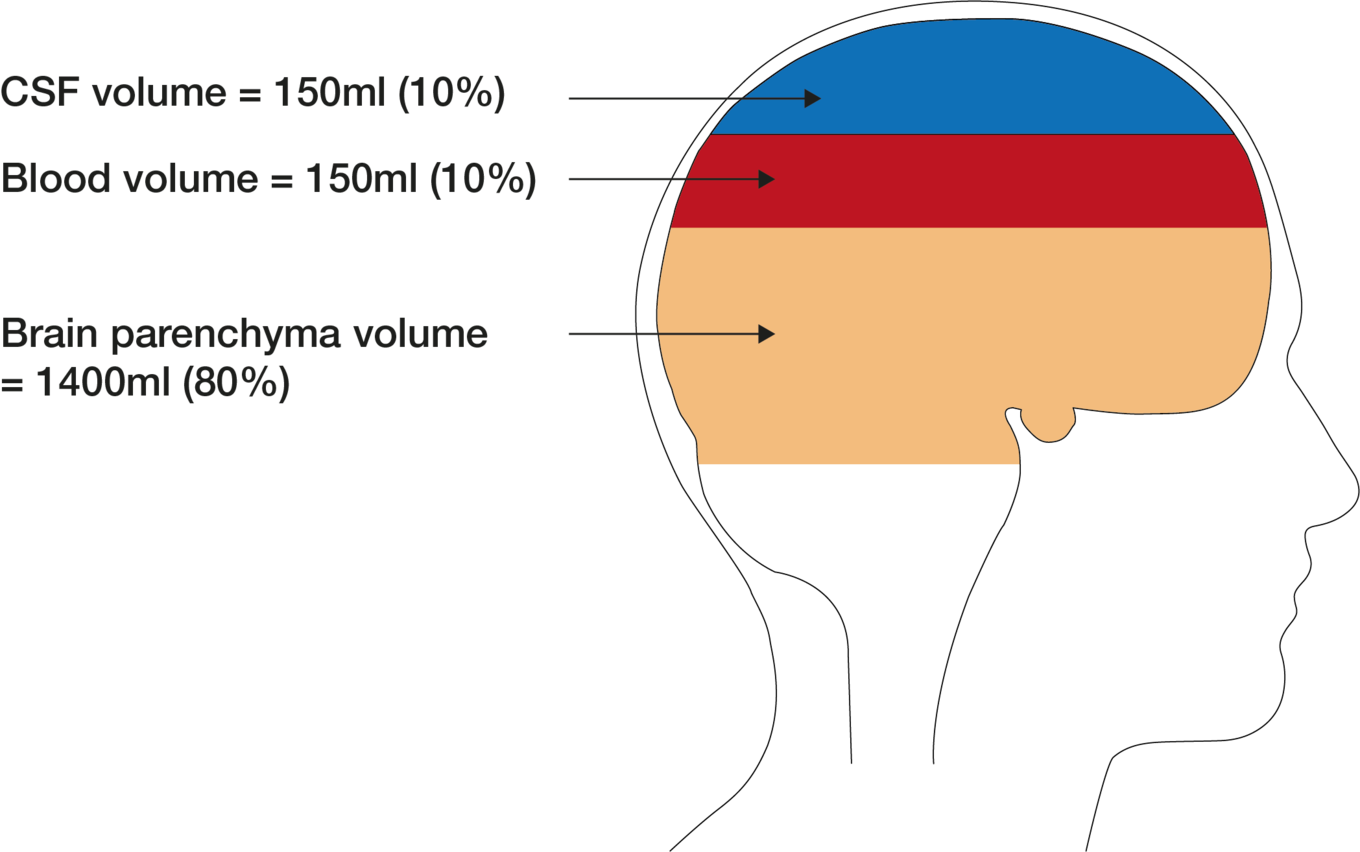
Anschaulich gesprochen reflektiert die Compliance etwas wie die „Weichheit“ oder „Elastizität“ des gesamten Schädel- und Spinalraumes. Diese Elastizität ist eine „Pseudo-Elastizität“, denn die Bestandteile Hirngewebe/Rückenmark, Blut und CSF sind für sich genommen inkompressibel, oder anders gesagt, „hart“. Die Compliance kommt so zustande, dass bei jeder zusätzlichen „Raumforderung“ innerhalb des harten Schädelvolumens – z.B. durch einen Aufstau von zu viel CSF (Hydrocephalus), bei einer Blutung (Hämatom) oder durch eine Geschwulst (Krebs, Zyste, Schwellung) – im Wesentlichen venöses Blut aus dem starren Raum nach außen in den Körper verdrängt wird. So steigt der Druck im Schädel (ICP = Intracranial pressure) durch solche Raumforderungen bei normaler Compliance zunächst nur wenig an, weshalb diese auch oft mit einer „Druck-Reserve-Kapazität“ assoziiert wird. Wird die Raumforderung jedoch zu groß, so ist auch die Reservekapazität bald erschöpft und der ICP steigt stark an. Eine Minderung der Compliance ergibt sich aber nicht nur durch eine zu hohe Raumforderung, sondern auch durch pathologische Verhärtung des Gewebes und der Gefäße, vor allem der Venen (Sklerose). Man sagt, die Bestimmung der Compliance hat auch einen „diagnostischen Wert“, denn man erfährt durch sie etwas über die Höhe der Raumforderung und den Zustand des Gewebes bzw. der Blutgefäße.
Die exakte medizinische Definition der Compliance als Druck-Volumen-Beziehung (C = dV/dP) ist in der folgenden Druck-Volumen-Kurve erläutert:
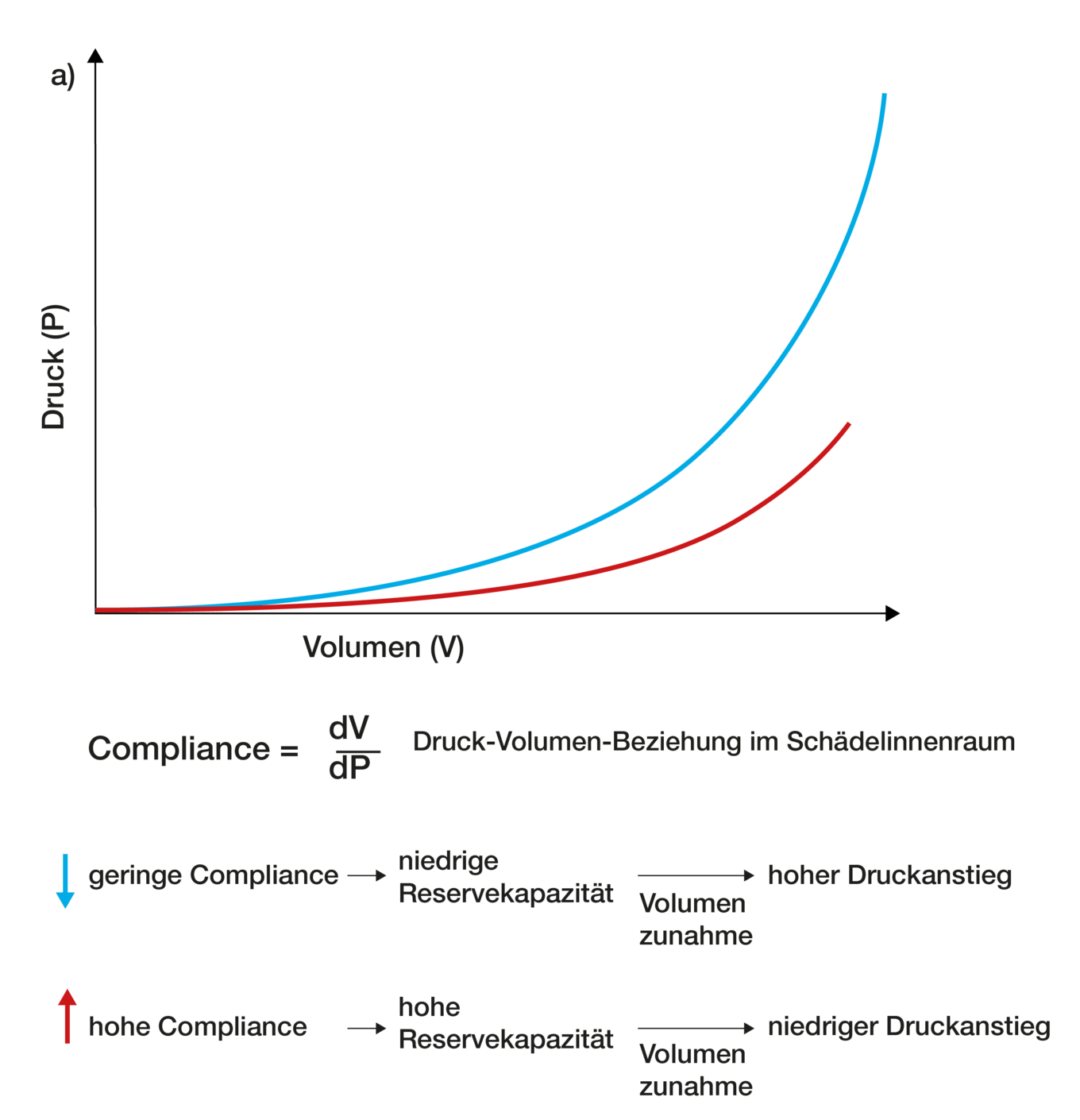
Eine besondere physiologische (natürliche/gesunde) Raumforderung im Schädelinnenraum ergibt sich aus dem periodischen wellenartig Einströmen des arteriellen Blutes. In der folgenden Figur wird illustriert, wie die Amplitude (d.h. die Höhe) der immer vorhandenen ICP-Pulswellen von der Compliance abhängt: hohe ICP-Wellenamplituden zeigen eine verringerte Compliance.
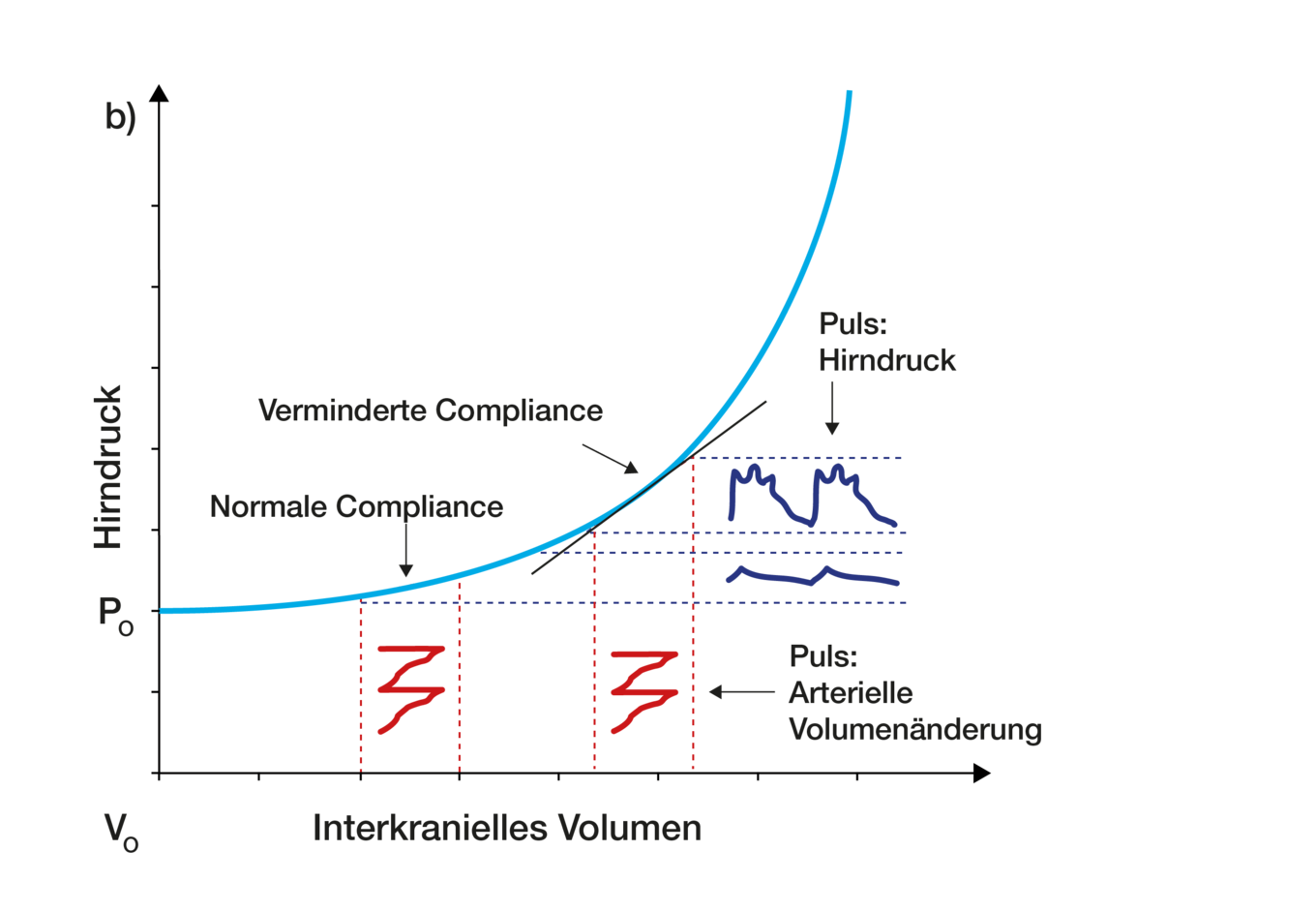
Zwar befinden sich nur wenige Prozent der gesamten CSF-Menge im knöchernen Spinalkanal, dafür aber umso mehr venöses Blut (d.h. Venen). Der „durale Sack“, in dem sich das spinale CSF befindet, ist dehnbar und weitet sich im Stehen durch das Absacken von CSF aus dem Schädel nach unten deutlich auf. Insgesamt trägt der Spinalkanal wahrscheinlich zu mehr als 50% zur gesamten Compliance bei.
Die Überdrainage ist nicht so einfach erklärbar wie die Unterdrainage. Wie kann ein Sog solcher Größenordnung allein durch die Shunt-Implantation entstehen, d.h. durch die künstliche Verbindung der Ventrikel mit dem (vorwiegend) Bauchraum? Der einzige Bereich im menschlichen Körper, in dem ein gewisser moderater Unterdruck (negativer Druck, Sog) herrscht, ist der Pleuraspalt (p = approx. - 5cmH2O), aber der wird als Ableitungsort für die Drainage heutzutage kaum noch in Betracht gezogen. Es gab früher auch Spekulationen über einen „dynamischen Pumpmechanismus“, z.B. bei schreienden Kindern, die sich aber nicht bestätigen ließen.
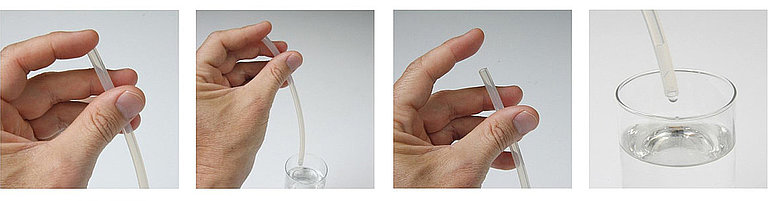
Eine plausible hinreichende Erklärung findet sich jedoch im sogenannten hydrostatischen Druck (englisch: Hydrostatic Pressure = HSP). Dieser tritt ausschließlich – dann aber zwangsläufig – in stehender Position des Patienten auf und wird durch das Gewicht der sich im Shunt (d.h. vor allem im langen Peritoneal-Katheter) befindlichen Flüssigkeitssäule hervorgerufen. Am unteren Ende des Katheters macht sich dieses Gewicht als Gewichtsdruck der Flüssigkeitssäule bemerkbar, am oberen Ende aber als Sog das ist der hydrostatische Druck (HSP), bzw. je nach Referenzpunkt, hydrostatische Sog. Ohne Ventil läuft die Flüssigkeitssäule einfach aus dem oben und unten offenen Katheter heraus, wobei dieser Vorgang durch das Gewicht der Flüssigkeit getrieben wird. Mit anderen Worten: wenn der Patient aufrecht steht und die obenliegenden Ventrikel über den langen Katheter mit dem untenliegenden Bauchraum verbunden sind, „möchten“ sich diese vollständig entleeren. Man kann das auch so ausdrücken, dass sie „leergesaugt“ werden, weshalb dieser Effekt häufig mit dem Begriff „Siphoning“ bezeichnet wird. Dieser extreme Fall würde allerdings nur dann eintreten, wenn Luft von außen in die Ventrikel nachströmen könnte. Da die Ventrikel aber normalerweise geschlossen sind, fließt nur so viel Liquor ab, bis der hydrostatische Sog durch eine im Hirngewebe entstehende Zugspannung („Gegensog“) ausgeglichen wird: wieviel das im Einzelfall ist, hängt u.a. von der Elastizität des Gewebes (Compliance) und von der Größe des Soges ab.
Hydrostatischer Druck in cmH2O
Der Druck im Liquor cerebrospinalis wird im medizinischen Fachjargon in der nicht-SI-Einheit („SI“ steht dabei für Système international d’unités und bezeichnet das internationale Einheitssystem für physikalische Größen) cmH2O ausgedrückt - gesprochen: „Zentimeter-Wassersäule“. Es ist ein sogenannter Differenzdruck, der den Druckunterschied (d.h. die Druckdifferenz) zwischen Schädelinnerem und äußerem Luftdruck beschreibt.
Ein cmH2O ist definiert als der hydrostatische Druck, den eine Wassersäule von einem Zentimeter Höhe bei einer Dichte von exakt einem Gramm pro Kubikzentimeter Wasser bewirkt. Anders als bei der für Druck üblichen Einheit Pa - gesprochen: „Pascal“ - die definiert ist als die Kraft eines Newtons, die auf eine Fläche von einem Quadratmeter wirkt, handelt es sich bei der Einheit cmH2O um eine Größe, die ganz ohne Wirkfläche auskommt. Sie bezieht sich lediglich auf ein eindimensionales Längenmaß, nämlich die Höhe der Wassersäule, die auf dem betrachteten Druckpunkt lastet. Dies entspricht nicht unserem intuitiven Verständnis von Druck, verdeutlicht dafür jedoch umso mehr die Wirkung des hydrostatischen Drucks – also dem Druck in einem Medium (z.B. in einer Flüssigkeit), der durch das Eigengewicht dieses Mediums selbst hervorgerufen wird. In anderen Worten: der Druck entsteht, weil das Medium mit seinem eigenen Gewicht auf sich selber drückt.
Ein cmH2O entspricht in etwa einem Millibar oder in SI-Einheiten ausgedrückt: tausend Pascal.
Der Hydrostatische Druck wird nach der Formel:
HSP = rho * g * h
berechnet. Dabei ist h die Höhe der Flüssigkeitssäule und rho und g physikalische Konstanten.
Bei einem durchschnittlichen Erwachsenen kann somit ohne Weiteres einen Sog von - 50 cmH2O erreicht werden. Dass die Verjüngung der Ventrikel die genannte starke Zugspannung erzeugt, liegt daran, dass das Gehirn an seiner Außenseite fest mit dem Schädel verbunden ist und daher nicht insgesamt „schrumpfen“ kann.
Dieser physikalischen Formel gemäß verschwindet dieser Effekt in liegender Position, denn die Höhe der Säule beträgt hier ja h = 0 cm, also auch HSP = 0. Das ist auch anschaulich ganz plausibel, denn die Flüssigkeitssäule im „liegenden“ (horizontalen) Katheter wird jetzt nicht mehr durch ihr Eigengewicht seitlich aus den Katheter-Enden herausgepresst. Mit anderen Worten: mit dem Bauchraum verbundene Ventrikel werden im Liegen auch nicht mehr leergesaugt. Der „Siphon-Effekt“ ist in dieser Lage nicht mehr vorhanden.
Es sei an dieser Stelle nochmal betont, dass dieser physikalische Effekt IMMER und UNVERMEIDLICH im Stehen auftritt, und – je nach Größe des Patienten bzw. je nach Abstand der Ventrikel vom Zwerchfell – einen massiven Sog von 20 - 60 cmH2O erzeugt. Dieser ist dann ohne Weiteres in der Lage, die oben beschriebenen Symptome wie Schlitzventrikel und sogar die räumliche Verschiebung von ganzen Hirnteilen hervorzurufen. Aus dieser rein physikalischen Erklärung wird auch klar, dass im Unterschied zur Unterdrainage, die an sich ganz ähnlichen Überdrainagesymptome NUR im Stehen auftreten, im Liegen aber relativ rasch wieder abklingen. Dies bietet ein gutes diagnostisches Unterscheidungskriterium zwischen beiden Phänomenen.
Das kritische Problem bei der Überdrainage ist also nicht primär der niedrige, intraventrikuläre Druck, sondern die Tatsache, dass durch die Dehnung des Hirngewebes die Bildung von Hygromen und Hämatomen, d.h. flüssigkeits- und blutgefüllten Hohlräumen vor allem zwischen Hirn-Oberfläche und Schädel gefördert wird. Das Gehirn ist über die fein-strukturierte sogenannte „Spinngewebshaut“ (Arachnoidea) und die Dura-Mater fest mit dem Schädel verbunden und kann sich normalerweise nicht von diesem lösen. Entsteht nun ein zu großer Sog nach innen, also von der Schädelwand weg, ist es zuerst diese feine Haut und die in ihr verlaufenden dünnen Brückenvenen, die reißen und einbluten. Es können aber auch große venöse Sinusgefäße in der Dura oder Arterien verletzt werden. Durch die Überdrainage werden fast ausschließlich sogenannte "Subdurale Hämatome" (SDH) hervorgerufen und diese können sogar chronisch werden. Laborexperimente belegen eindrucksvoll wie ein typischer hydrostatischer Sog in den Ventrikeln von ca. - 30 cmH2O an den fixierten äußeren Hirnhäuten Kräfte von mehreren hundert Gramm (Gewichtsäquivalent) hervorrufen kann. In dem beschriebenen Szenario ist es klar, dass Überdrainage-Hämatome sogar chronisch werden können (cSDH = chronical subdural haematoma).
Ein anderes durch die Überdrainage induziertes und ebenso gravierendes Problem ist das sogenannte Schlitzventrikelsyndrom. Durch das sog-induzierte Zusammenziehen der Ventrikel werden die feinen Öffnungen des Ventrikelkatheters (VK) verschlossen. Der Liquor kann nicht mehr abgeführt werden und die Ventrikel weiten sich wieder. Wird der Sog danach erneut wirksam, beginnt der Prozess von vorne. Diese periodische, mit starken Spannungen verbundene Kontraktion und Expansion der Ventrikel kann das Gewebe bereits schädigen. Wächst dann noch Gewebe in die kleinen Katheterlöcher ein, kann dies bei der nachfolgenden Ventrikelexpansion ebenfalls zu Geweberissen und kleinen Blutungen führen. Die Innenseite der Ventrikel – das Ependym – vernarbt und die Ventrikel „erstarren“. Dies ist u.a. ein Grund dafür, dass die Ventrikelweite kein eindeutiges Maß für die vorliegenden Druckverhältnisse ist.
Das Ventil ist sehr häufig retroauriculär, d.h. auf der Höhe der Ventrikel implantiert. Die Bezeichnung „Sog“ macht hier besonders deutlich, dass der negative HSP „unterhalb“ des Ventils durch die hängende Flüssigkeitssäule hervorgerufen wird und nichts mit dem pathologischen Überdruck in den Ventrikeln zu tun hat. Der hohe Sog im Stehen lässt sich immer durch einen besonders hohen Öffnungsdruck (OPmax) des Ventils kompensieren und daher ist das Hochstellen des Ventils durch den behandelnden Arzt auch die erste Gegenmaßnahme, wenn eine Überdrainage vermutet wird. Bei erhöhtem intraventrikulärem Druck (IVP) öffnet das Ventil und reduziert diesen so lange, bis die Summe aus IVP und HSP den Öffnungsdruck des Ventils wieder unterschreitet. Der IVP wird durch die Flüssigkeitsabfuhr reduziert, aber der Sog im Katheter (Höhe h!) bleibt dabei immer konstant. Die Ventrikel werden auf diese Weise sozusagen vom Sog abgeschirmt und sind geschützt.
Im Liegen ist jedoch kein Sog mehr vorhanden (HSP = 0 cmH2O), aber das hochgestellte Ventil öffnet weiterhin nur dann, wenn die Summe aus IVP und Sog den Öffnungsdruck übersteigt. In Formeln ausgedrückt bedeutet das:
IVP + HSP = IVP + HSP LIEGEN = IVP + 0 > OP MAX
Diese Konstellation führt notwendig zu einem unter Umständen massiven Überdruck, d.h. zu einer deutlichen Unterdrainage. Um gegenzusteuern, müsste - wie eingangs bereits erwähnt - der Öffnungsdruck wieder auf einen niedrigen Wert OPmin gesenkt werden, aber dann wird der Sog im Stehen nicht mehr kompensiert: in dieser Konstellation wäre das Ventil permanent geöffnet und eine Überdrainage die unvermeidliche Folge. Die Schlussfolgerung ist also, dass mit einem einfachen Ventil - je nach Typ oder Einstellung - zwangläufig eine Über- oder eine Unterdrainage auftritt (Bergsneider3, 2004).
Physiologischer und pathologischer Hirndruck – Wann ist es zu viel? Wann zu wenig?
Der intraventrikuläre Druck (IVP) ist auch beim gesunden Menschen keine Konstante: durch Luftanhalten oder Pressen steigt er deutlich an. Puls- und atmungsinduzierte Druckwellen sind neben einigen anderen immer vorhanden. Neben personenspezifischen, tages- und situationsspezifischen Schwankungen ist er im Liegen generell leicht positiv und im Stehen leicht negativ. Dieser physiologische (d.h. normale) Unterdruck im Stehen wird durch das Absacken des Hirnwassers in den Spinalkanal hervorgerufen und gleicht insofern dem oben beschriebenen, durch den Peritonealkatheter hervorgerufenen hydrostatischen Sog. Der durch den Spinalkanal erzeugte physiologische Sog wird allerdings durch verschiedene natürliche Mechanismen deutlich reduziert. Einerseits ist dieser Kanal nicht wie der Katheter nach unten hin geöffnet und der Liquor kann deshalb gar nicht ablaufen, sondern nur im Stehen nach unten hin „absacken“. Der Spinalkanal hat nämlich genau wie die Ventrikel und das Gehirnparenchym eine gewisse Elastizität (Compliance).
Ein weiterer Mechanismus, der ein zu starkes Abfallen des intraventrikulären Druckes im Stehen verhindert, ist der „Kollaps der Jugularvenen“, die vom Hirn zum Herzen nahe unter der Halsoberfläche entlang führen. Außer im Halsbereich sind die Venen nämlich im ganzen Körper und im Gehirn („Sinus sagittalis“) mit dem umgebenden Gewebe verspannt, so dass sie nicht zusammenfallen können. Der Halsbereich ist die einzige Stelle, wo sie sich schon bei leichtem negativen Druck im Stehen zusammenziehen („kollabieren“). Ergo: auch das venöse Blut stellt eine hydrostatische Säule dar. Ist der venöse Blutfluss erst unterbrochen, steigt der venöse Hirndruck und mit ihm der intraventrikuläre Druck wieder an.
Das Gehirn ist jedenfalls auf deutliche Druckschwankungen ausgelegt und kann diese sehr gut tolerieren. Wahrscheinlich ist sogar - wie bei fast jedem biologischen Zellgewebe - eine bestimmte „Bewegung“ wünschenswert und physiologisch sinnvoll. Konkret fürs Hirngewebe könnte die durch die Druckschwankungen hervorgerufene Kompressions- und Zugspannung im Parenchym für den Transport von Nährstoffen und das Abführen von Stoffwechselprodukten hilfreich oder sogar notwendig sein.
Ein gewisser Unterdruck in den Ventrikeln muss also nicht per se „schädlich“ sein. Entscheidend ist am Ende weder irgendein ICP-Lehrbuch-Wert (den es gesichert und allgemein akzeptiert bisher gar nicht gibt (Pedersen4, 2018)) noch die absolute Weite der Ventrikel im MRT-Bild. Entscheidend ist allein die Frage, ob der Patient beschwerde- und symptomfrei ist und sich wohl fühlt. Es hat sich über lange Zeiträume gezeigt, dass der „optimale” Hirndruck von Patient zu Patient sehr variabel ist (Antes5, 2018). Beispielsweise hat sich für die spezielle Gruppe der sogenannten „NPH-Patienten“ (englisch: Normal Pressure Hydrocephalus = NPH) seit der großen Studie von Boon und Mitarbeitern im Jahre 1998 (Boon6, 1998; Malem7 2014) die Etablierung eines besonders niedrigen (vermutlich unphysiologischen?) Hirndruckes als zuträglich für ein „positives klinisches Outcome“ erwiesen.
In den letzten Jahren scheinen lumbo-peritoneale Shunts (LP-Shunts) immer beliebter zu werden, da hier Schädel und Gehirn nicht verletzt werden müssen. Beim LP-Shunt wird der Liquor vom Spinalkanal, der direkt mit den Ventrikeln verbunden ist, zwischen dem dritten und fünften Lendenwirbelkörper (LWK) ins Peritoneum abgeleitet. Bis heute wird in der Literatur manchmal die Ansicht vertreten, beim LP-Shunt spiele der hydrostatische Sog keine bedeutende Rolle und die Gefahr einer Überdrainage sei hier deutlich kleiner (Bloch8, 2012). Diese vollkommen falsche und irreführende Aussage entsteht wahrscheinlich durch den Umstand, dass beim LP-Shunt Liquorquelle (Spinalkanal) und Drainageort (Peritoneum) nicht übereinander, sondern „scheinbar auf gleicher Höhe“ liegen: der Shunt-Katheter zwischen Punktionsort und Bauchraum liegt ja tatsächlich im Mittel horizontal, so dass die hydrostatische Höhe h = 0 zu sein scheint.

Wie bereits weiter oben erklärt wurde, erhebt sich aber im Stehen der gesamte liquorgefüllte Spinalkanal bis hin zu den Ventrikeln über dem Bauchraum. Durch den Shunt ist der Kanal nun allerdings geöffnet, die spinale Flüssigkeitssäule kann in den Bauchraum abfließen und in den Ventrikeln entsteht dabei exakt der gleiche hydrostatische Sog (der Höhe h) wie im Falle eines ventriculo-peritonealen Shunts. Da der Spinalkanal wesentlich breiter als der dünne Peritonealkatheter ist und der Liquorfluss somit größer, tritt die Überdrainage sogar deutlich schneller ein. In einer aktuellen Übersichtsarbeit (Miyake9, 2016) wird die ähnliche, missverständliche Bemerkung gemacht, „der Siphon-Effekt sei für LP-Shunts zu vernachlässigen“. Dies ist differenziert zu betrachten: „aus Sicht des LP-Ventiles“, das ja auf der Höhe des Bauchraumes liegt, ist tatsächlich kaum Sog vom Bauchraum (d.h. „von unten“) her vorhanden. Dafür lastet allerdings zusätzlich zum IVP der gesamte hydrostatische Druck des Spinalkanales „von oben“ auf ihm. Beim VP-Shunt ist es umgekehrt: das Ventil liegt auf Höhe der Ventrikel und „von unten“ zieht der gesamte hydrostatische Sog, wohingegen „von oben“ nur der vergleichsweise geringe IVP einwirkt. Für die Öffnung eines herkömmlichen Differenzdruckventiles ist jedoch ausschließlich die Summe aus beiden Druck/Sog-Anteilen relevant. Zur Überdrainage kommt es daher in beiden Fällen gleichermaßen.
Außer vorliegenden Indizien und Plausibilitätsüberlegungen ist es in den letzten Jahrzehnten noch nicht gelungen, die Über- oder Unterlegenheit eines bestimmten Ventiltyps zweifelsfrei nachzuweisen. Die normalerweise geradezu dahinrasende naturwissenschaftliche Erkenntnis scheint hier langsam wie eine Schnecke zu kriechen. Neben vielen anderen gewichtigen Gründen hat dies sicherlich auch damit zu tun, dass die menschliche Physiologie äußert kompliziert ist und sich belastbare statistische Aussagen meist nur mit massivem Aufwand gewinnen lassen. Deshalb soll insbesondere der differenzierten Abwägung der Vor- und Nachteile der verschiedenen marktgängigen hydrostatischen Implantate in einem späteren Kapitel genügend Raum eingeräumt werden.
Dennoch kann und soll für die Gravitationsventile an dieser Stelle bereits gesagt werden, dass ihre effektive Wirksamkeit bei der Vermeidung von Überdrainage in der wissenschaftlichen Literatur sehr gut belegt ist, und dies für jede Altersgruppe. Die folgende Liste an jüngeren Studien ist dabei nur als Auswahl zu verstehen: Al-Hakim10, 2018; Gebert11, 2016; Xinxing12, 2015; Suchorska13, 2015; Kehler14, 2015; Malem7, 2014; Thomale15, 2013; Lemcke16, 2013; Gebert17, 2013; Freimann18, 2013.
Ein Ergebnis der unter Neurochirurgen gut bekannten SVASONA Studie (Lemcke16, 2013) ist, dass eine Überdrainage bei jedem dritten Patienten mit Gravitationsventilen vermieden werden kann. Zwar ist in dieser Studie die Überdrainagerate „in der Kontrollgruppe“ (d.h. in der Gruppe, in der keine Gravitations-Ventile implantiert wurden) deutlich höher als in anderen Studien (Sundstrom19, 2017), aber nichts desto Trotz die entsprechende Rate in der Therapiegruppe (mit Gravitations-Ventilen) auch auffällig klein. Dass dies für viele Therapiegruppen mit Gravitations-Ventilen gilt, hat gerade Alfred Aschoff, ein bei Neurochirurgen bekannter Hydrocephalus-Experte, in seinem jüngst erschienen Lehrbuch-Kapitel über Shunt-Ventile (Aschoff20, 2019) angemerkt.
In diesem reichhaltigen Text hat Aschoff auch die sogenannten „Überlebenskurven“ (oder auch Kaplan-Meier-Kurven) für verschiedene Ventile „übereinander gelegt“, um sie direkt zu vergleichen. „Überlebenskurven“ sind in der Shunttherapie weit verbreitet, denn sie zeigen graphisch, wie viele (in Prozent) der anfänglich implantierten Ventile nach einer bestimmten Zeit noch „überlebt“ haben, d.h. weiterhin fehlerfrei arbeiten. Die übrigen wurden revidiert, d.h. wegen einer Fehlfunktion oder Komplikation operativ entfernt. Eine wichtige, unter Umständen irreversible Komplikation ist eben auch die hier diskutierte Überdrainage, die somit zu einer verkürzten Lebens/Funktionszeit des Ventiles beiträgt. Andere wichtige Gründe für ein Shuntversagen sind Infektionen, Verstopfungen und mechanische Fehlfunktionen, wie Bruch des Ventils oder Abreißen des Katheters. In den von Aschoff miteinander verglichenen Überlebenskurven stammen die oberen Kurven alle aus Studien mit Gravitations-Ventilen: im Unterschied zu den herkömmlichen Vergleichsventilen, bei denen nach 2 Jahren nur noch ca. 50-60% fehlerfrei arbeiten, sind bei den Gravitations-Ventilen nach derselben Zeit noch ca. 80% vorhanden.
Die von Aschoff gefolgerte „Überlegenheit der Gravitations-Ventile“ hat sich ebenfalls in den offiziellen Leitlinien für die „Diagnostik und Therapie des Normaldruckhydrozephalus“ niedergeschlagen, die von der Deutschen Gesellschaft für Neurologie periodisch herausgegeben werden:
www.awmf.org/uploads/tx_szleitlinien/030-063_S1_Normaldruckhydrozephalus_2018-03.pdf
Dort heißt es unter der Rubrik „Wichtige Empfehlungen“:
„Wenn zur Behandlung des iNPH ein ventrikuloperitonealer Shunt gelegt wird, sollte ein gravitationsabhängiges Ventil implantiert werden. Differenzialdruckventile mit verstellbarem und insbesondere mit nichtverstellbarem Ventilöffnungsdruck führen bei gleichem klinischem Effekt signifikant häufiger zu Überdrainage-Komplikationen“.
Literaturverzeichnis
1) 2007, Ritz R., Roser F., Morgalla M., Dietz K., Tatagiba M. and Will B. E.: "Do antibiotic-impregnated shunts in hydrocephalus therapy reduce the risk of infection? An observational study in 258 patients",
BMC Infect Dis 7: 38,
Abstr.: BACKGROUND: Shunt infection in hydrocephalus patients is a severe, even life-threatening complication. Antibiotic-impregnated shunts (AIS) have been developed in an attempt to reduce rate of shunt infection. The study was performed to analyze if AIS can diminish the rate of shunt infection. The pathogenic nature of shunt infection in patients with AIS systems and those without antibiotic impregnated shunts (non-AIS) was compared. METHODS: Over a period of 24 months in the Department of Neurosurgery at University Hospital of Tubingen shunt surgery was performed in 258 patients. In 86 patients AIS systems were implanted. Shunt catheters were commercially impregnated with clindamycin and rifampicin. Analysis of the clinical data included sex, age, classification of hydrocephalus, shunt types and risk factors for shunt infection [age (< 1 year and > 80 years), prematurely born patients, external ventricular drainage, former shunt infection, former systemic infection, disturbance of consciousness, former radiation-/chemotherapy]. Infection rates and underlying bacterial pathogens of patients with AIS were compared to patients with implanted non-AIS systems (172 patients). RESULTS: AIS and non-AIS patients did not differ in sex, etiology of hydrocephalus and the shunt type. In the AIS group 72 out of 86 patients had at least one risk factor (83.7 %), compared to 126 patients in the non-AIS group (73.3 %). There was no significant difference between the two groups (p = 0.0629; Fisher's exact test). In patients with no risk factors, only one patient with non-AIS suffered from shunt infection. In patients with one or more risk factors the rate for shunt infection was 7.14 % in patients with non-AIS and 6.94 % in patients with AIS. Former shunt infection (p = 0.0124) was related to higher risk for shunt infection. The use of AIS had therefore no significant advantage (p = 0.8611; multiple logistic regression). Significantly related to a shunt infection was the number of shunt surgeries. 190 interventions in the AIS group (2.21 interventions per patient) and 408 in the non-AIS group (2.37 interventions per patient) had been performed (p = 0.3063; Wilcoxon). There was no shunt infection in the group of patients on whom only one shunt surgery was performed. In patients with at least two shunt surgeries the infection rate was 9%. The infection rate in AIS patients was 5/52 (9.6 %) and in the non-AIS 10/114 (8.77 %), (p = 1.0; Fisher's exact test). Staphylococcus epidermidis was the most frequent pathogen for shunt infection. Fourteen out of 15 infections occurred within the first 6 months of surgery. The most frequent pathogen for shunt infection was S. epidermidis. No toxic or allergic complications were seen using the AIS shunt systems. The presented data show a remarkably low infection rate of 5.8 % in the non-AIS group compared to other studies which demonstrated a significant decrease in the infection rate by AIS. CONCLUSION: AIS did not significantly reduce shunt infection in hydrocephalus patients in the presented study. In the AIS group three patients suffered from shunt infections caused by skin ulceration or neurosurgical procedures with exposure of the cerebrospinal liquor after shunt implantation. AIS was not developed to prevent infection in such cases, therefore an advantage of AIS can not be excluded. In view of the presented data and the small number of reported studies a prospective randomized multicenter study is required.
2) 2015, Feb, Parker S. L., McGirt M. J., Murphy J. A., Megerian J. T., Stout M. and Engelhart L.: "Comparative effectiveness of antibiotic-impregnated shunt catheters in the treatment of adult and pediatric hydrocephalus: analysis of 12,589 consecutive cases from 287 US hospital systems",
J Neurosurg 122(2): 443-448,
Abstr.: OBJECT: The real-world effectiveness of antibiotic-impregnated shunt catheters to reduce the incidence of shunt infections is still debated. The literature to date consists mostly of small, single-institution studies. The aim of this study was to assess the incidence of infection for antibiotic-impregnated catheters (AICs) versus standard shunt catheters in a large nationwide administrative database. METHODS: The authors retrospectively reviewed hospital discharge and billing records from the Premier Perspective Database from April 2003 to July 2009 to identify all adult and pediatric patients undergoing de novo ventricular shunt placement. The primary end point was the incidence of shunt infection within 1 year of implantation. Multivariate logistical regression was performed to determine factors associated with increased incidence of infection. RESULTS: A total of 10,819 adult (AIC, 963; standard catheter, 9856) and 1770 pediatric (AIC, 229; standard catheter, 1541) patients underwent ventricular shunt placement in 287 US hospitals. Overall, the incidence of infection was 3.5% in adults (n=380) and 6.6% in pediatric patients (n=116). AICs were associated with significant reduction in infection for both adult (2.2% vs 3.6%, p=0.02) and pediatric (2.6% vs 7.1%, p<0.01) patients. AIC use was associated with reduced infection regardless of hospital size, annual shunt volume, hospital location, or patient risk factors and remained associated with a reduced infection in multivariate analysis for both adult (p=0.02) and pediatric (p=0.02) patients. CONCLUSIONS: The use of antibiotic-impregnated shunt catheters was associated with a reduction in shunt infections for both adult and pediatric patients. This provides further support that AICs may represent a reliable means of reducing shunt infections for both adult and pediatric patients.
3) 2004, Oct, Bergsneider M., Yang I., Hu X., McArthur D. L., Cook S. W. and Boscardin W. J.: "Relationship between valve opening pressure, body position, and intracranial pressure in normal pressure hydrocephalus: paradigm for selection of programmable valve pressure setting",
Neurosurgery 55(4): 851-858; discussion 858-859,
Abstr.:OBJECTIVE: There is little scientific basis for guidance in selecting the optimal valve for the treatment of normal pressure hydrocephalus. The aim of this study was to determine the programmable valve opening pressure setting that would result in a slight reduction in intracranial pressure (ICP) after a ventriculoperitoneal shunt is implanted. We also assessed whether shunt-induced ICP could be predicted on the basis of a simple hydrodynamic equation. METHODS: In this prospective study of 11 patients with normal pressure hydrocephalus, ICP was measured before and after implantation of a shunt incorporating a programmable valve without an antisiphon device. Pressure measurements, including intraperitoneal pressure, were recorded at body angles ranging from 0 to 55 degrees and at valve settings ranging from 30 to 200 mm H(2)O. Measured ICP values were compared with values computed using a simple hydrodynamic equation. RESULTS: Even at a valve setting greater than the mean baseline ICP (200 mm H(2)O), the supine ICP was significantly lower than the baseline value (baseline ICP, 164 +/- 64 mm H(2)O; postoperative ICP, 125 +/- 69 mm H(2)O, P = 0.04). Valve pressure did not equate 1:1 with the measured postoperative ICP. Comprehensive ICP measurements at upright body positions demonstrated a stepwise reduction in ICP rather than a precipitous decline as a result of so-called siphoning. CONCLUSION: This study indicates that very high valve opening pressure settings may be optimal for the initial treatment of normal pressure hydrocephalus. The relationship between ICP and opening pressure valves is linear but not predicted by simple hydrodynamics.
4) 2018, Feb, Pedersen S. H., Lilja-Cyron A., Andresen M. and Juhler M.: "The Relationship Between Intracranial Pressure and Age-Chasing Age-Related Reference Values",
World Neurosurg 110: e119-e123,
Abstr.: BACKGROUND: No true reference values for intracranial pressure (ICP) in humans exist; current values are estimated from measurements in adults who undergo treatment in order to correct ICP. We report ICP values in a "pseudonormal" group of children and adults to examine if age affects ICP. METHODS: We analyzed data from all nonshunted patients undergoing a 24-hour ICP monitoring as part of a diagnostic work-up and included patients with no subsequent suspicion of increased ICP and no need for pressure-relieving treatment with a minimum follow-up period of 3 years. RESULTS: From February 2008 to November 2014, a 24-hour ICP monitoring was performed in 221 patients. Of these patients, 35 (14 children, 21 adults) met the inclusion criteria. Follow-up time to confirm absence of ICP-related disease was 3-9 years. Daytime ICP was 2.8 mmHg +/- 2.2 in children and 1.9 mmHg +/- 4.2 in adults (P = 0.39). Of 35 patients, 32 had higher nighttime ICP. The difference between daytime and nighttime ICP was similar in children (DeltaICP = 5.8 mmHg +/- 4.0, P < 0.0001) and adults (DeltaICP = 6.1 mm Hg +/- 3.3, P < 0.0001). ICP could be described as a decreasing function of age, with an ICP decrement of 0.69 mmHg per decade (P = 0.015). CONCLUSIONS: We found similar differences in daytime and nighttime ICP between children and adults with no ICP-related disease. ICP seems to decrease with age across all ages. This has implications for therapeutic interventions (e.g., shunt valve selection or resistance in external ventricular drainage).
5) 2018, Jan, Antes S., Stadie A., Muller S., Linsler S., Breuskin D. and Oertel J.: "Intracranial Pressure-Guided Shunt Valve Adjustments with the Miethke Sensor Reservoir",
World Neurosurg 109: e642-e650,
Abstr.: BACKGROUND: Telemetric intracranial pressure (ICP) monitoring seems to be a promising therapy-supporting option in shunt-treated patients. Benefits become obvious when headaches are unspecific and clinical symptoms cannot be related to possible overdrainage or underdrainage. In this study, we evaluated a new telemetric device to individually adjust shunt valves according to ICP measurements. METHODS: Between December 2015 and November 2016, 25 patients with suspected suboptimal shunt valve settings underwent insertion of a telemetric ICP sensor (Sensor Reservoir; Christoph Miethke, Potsdam, Germany). Over a 1-year period, a total of 183 telemetric ICP measurements and 85 shunt valve adjustments were carried out. Retrospective statistic analyses focused on valve adjustments, ICP values, and clinical outcomes. RESULTS: ICP-guided valve adjustments positively changed the clinical state in 18 out of 25 patients. Clinical improvement over time was associated with significant changes of the valve settings and ICP values. Interestingly, a therapeutically normalized ICP profile was not automatically associated with clinical improvement. CONCLUSIONS: The Sensor Reservoir is an important and valuable tool for shunt-treated patients suffering from drainage-related problems. The possibility to simultaneously recognize and solve shunt problems represents the decisive advantage. Nevertheless, measurements with the Sensor Reservoir did not allow for the determination of default valve settings or universal target ICP values.
6) 1998, Mar, Boon A. J., Tans J. T., Delwel E. J., Egeler-Peerdeman S. M., Hanlo P. W., Wurzer H. A., Avezaat C. J., de Jong D. A., Gooskens R. H. and Hermans J.: "Dutch Normal-Pressure Hydrocephalus Study: randomized comparison of low- and medium-pressure shunts",
J Neurosurg 88(3): 490-495,
Abstr.: OBJECT: The goal of this prospective study was to compare outcome after placement of a low- or medium-pressure shunt in patients with normal-pressure hydrocephalus (NPH). METHODS: Ninety-six patients with NPH were randomized to receive a low-pressure ventriculoperitoneal shunt (LPV; 40 +/- 10 mm H2O) or medium high-pressure ventriculoperitoneal shunt (MPV; 100 +/- 10 mm H2O). The patients' gait disturbance and dementia were quantified by applying an NPH scale, and their level of disability was evaluated by using the modified Rankin scale (mRS). Patients were examined prior to and 1, 3, 6, 9, and 12 months after surgery. Primary outcome measures were determined by differences between preoperative and last NPH scale scores and mRS grades. The LPV and MPV shunt groups were compared by calculating both the differences between mean improvements and the proportions of patients showing improvement. Intention-to-treat analysis of mRS grades yielded a mean improvement of 1.27 +/- 1.41 for patients with LPV shunts and 0.68 +/- 1.58 for patients with MPV shunts (p = 0.06). Improvement was found in 74% of patients with LPV shunts and in 53% of patients with MPV shunts (p = 0.06) and a marked-to-excellent improvement in 45% of patients with LPV shunts and 28% of patients with MPV shunts (p = 0.12). All outcome measures indicated trends in favor of the LPV shunt group, with only the dementia scale reaching significance. After exclusion of serious events and deaths unrelated to NPH, efficacy analysis showed the advantage of LPV shunts to be diminished. Reduction in ventricular size was also significantly greater for patients in the LPV shunt group (p = 0.009). Subdural effusions occurred in 71% of patients with an LPV shunt and in 34% with an MPV shunt; however, their influence on patient outcome was limited. CONCLUSIONS: Outcome was better for patients who had an LPV shunt than for those with an MPV shunt, although most differences were not statistically significant. The authors advise that patients with NPH be treated with an LPV shunt.
7) 2014, Aug 21, Malem D. N., Shand Smith J. D., Toma A. K., Sethi H., Kitchen N. D. and Watkins L. D.: "An investigation into the clinical impacts of lowering shunt opening pressure in idiopathic normal pressure hydrocephalus: A case series",
Br J Neurosurg: 1-5,
Abstr.: Introduction. Idiopathic normal pressure hydrocephalus (iNPH) is a shunt- reversible syndrome of the elderly. Shunt management is aimed at achieving a balance between clinical improvement and the complications associated with overdrainage. Although clinical improvement occurs at low pressure, these benefits may be negated by the increase in complication rates observed at lower pressures. The addition of gravity-switch devices has been shown to reduce over drainage problems even at a low valve pressure setting. At our centre the Miethke proGAV is used and commonly lowered below 5 cmH2O to gain further clinical improvement. Object. To determine whether lowering the opening pressure to below 5cmH2O using the proGAV valve in iNPH patients results in a) improved clinical features; and b) no significant increase in complication rates. Methods. A retrospective case series of iNPH patients was undertaken with 24 patients who had the proGAV shunt system inserted with an initial opening pressure of 5cmH2O. Exclusion criteria were secondary NPH, shunt system other than proGAV inserted, no valve adjustment to below 5cmH2O and inadequate follow-up. Outcome measures were clinical improvement (gait, cognition and urinary continence) and complications (subdural haematoma, low-pressure symptoms and valve damage). Results. Patients underwent a total of 29 adjustments to below 5cmH2O. The mean valve opening pressure after the first adjustment was 2.5cmH2O and the mean opening pressure after the second adjustment was 1cmH2O. Overall, outcome after adjustment included 26% no change, 48% improvement and 26% deterioration clinically. One patient (4%) suffered traumatic subdural haematoma that resolved with increasing valve pressure to 20cmH2O. There was no valve damage or low-pressure symptoms after adjustment. Conclusion. This study found that lowering the opening pressure of the proGAV shunt system to below 5cmH2O results in clinical improvement and does not significantly increase the complication rate in iNPH patients.
8) 2012, Aug, Bloch O. and McDermott M. W.: "Lumboperitoneal shunts for the treatment of normal pressure hydrocephalus",
J Clin Neurosci 19(8): 1107-1111,
Abstr.: Ventriculoperitoneal shunt placement is the standard of care for idiopathic normal pressure hydrocephalus (iNPH). Studies have reported shunt complication rates up to 38%, with subdural hemorrhage rates as high as 10%. Lumboperitoneal (LP) shunts with horizontal-vertical valves (HVV) are an alternative for cerebrospinal fluid (CSF) diversion that avoids direct cerebral injury and may reduce the risk of overdrainage. Here we reviewed our experience with LP-HVV shunt placement for iNPH. We retrospectively reviewed our 33 patients with LP-HVV shunts inserted for the treatment of iNPH from 1998 to 2009. Patients were evaluated for improvements in gait, urinary function, and dementia after shunt placement. All patients had evidence of ventriculomegaly and a positive response to pre-operative lumbar puncture or extended lumbar drainage. All 33 (100%) patients had pre-operative gait dysfunction, 28 (85%) had incontinence, and 20 (61%) had memory deficits. Mean follow-up time was 19 months. Following shunt placement, 33/33 (100%) patients demonstrated improved gait, 13/28 (46%) had improvement in incontinence, and 11/20 (55%) had improvement in memory. Shunt failures requiring revision occurred in nine patients (27%), with an average time to failure of 11 months. Infections occurred in two patients (6%). There were no neurologic complications, including no hemorrhages. Thus, LP-HVV shunt placement is a safe and effective alternative to ventriculoperitoneal shunting for iNPH, resulting in significant symptomatic improvement with a low risk of overdrainage. It should be considered as an option for the treatment of patients with iNPH who demonstrate clinical improvement following lumbar drainage.
9) 2016, May 15, Miyake H.: "Shunt Devices for the Treatment of Adult Hydrocephalus: Recent Progress and Characteristics",
Neurol Med Chir (Tokyo) 56(5): 274-283,
Abstr.: Various types of shunt valves have been developed during the past 50 years, most of which can be classified into the following categories: (1) fixed differential pressure valves; (2) fixed differential pressure (DP) valves with an antisiphon mechanism; (3) programmable DP valves; (4) programmable DP valves with an antisiphon mechanism; and (5) programmable antisiphon valves. When considering the myriad of possible postoperative condition changes, such as the onset of accidental non-related diseases or trauma in adults, and changes in normal physiological development or anticipation of future shunt removal in children, it has become standard to use the programmable valve as a first choice for cerebrospinal fluid shunting. However, it is still unclear what type of shunt valve is suitable for each individual case. Based on the results of SINPHONI and more recently SINPHONI 2 trials, the programmable DP valve is recommended as the first line shunt valve. The programmable DP valve with an antisiphon mechanism is thought to be beneficial for tall, slender patients, who have a tendency for easily developing complications of overdrainage, however, this type of valve must be used cautiously in obese patients because of the increased risk of underdrainage. Although the current evidence is still insufficient, the programmable antisiphon valve, which costs the same as the programmable DP valve, is also thought to be the first line shunt valve. The quick reference table is applicable for most shunt valves, and for patients with either the ventriculoperitoneal or the lumboperitoneal shunt.
10) 2018, Jul, Al-Hakim S., Schaumann A., Schneider J., Schulz M. and Thomale U. W.: "Experience in shunt management on revision free survival in infants with myelomeningocele",
Childs Nerv Syst 34(7): 1375-1382,
Abstr.: OBJECTIVE: Depending on the etiology of hydrocephalus in childhood, the shunt therapy still remains challenging due to frequent shunt complications leading to possible revisions such as shunt infection or shunt malfunction. In myelomeningocele (MMC) patients who often require shunt therapy, higher revisions rates were reported. In a single-center retrospective study, experiences on shunt regimen on hydrocephalus associated with MMC are presented. METHODS: Data of 160 infant hydrocephalus cases younger than 1 year of age at the time of implantation were retrospectively reviewed from the hospital database. These patients received an adjustable differential pressure valve with gravitational unit and antibiotic impregnated catheters as a primary or secondary implant during the time period of April 2007 to July 2015. The subgroup of infants cases with MMC (n = 44; age 50.6 +/- 80.6 days) were compared to the remaining cohort of other hydrocephalus etiology (control group). The shunt and valve revision free survival rates were recorded until July 2017. RESULTS: During the mean follow-up of 48.7 +/- 19.2 (7-114) months, the shunt revision free survival was 87% at 1 year and 49% at 60 months in the MMC cohort. The control group showed a shunt survival rate of 68% at 1 year and 39% at 60 months. Similarly, the valve revision free survival rate showed a significant higher rate of 92% at 1 year and 69% at 60 months in the MMC group compared to the control group (75% at 1 year and 51% at 60 months; p < 0.05). During the entire follow-up period, 37% of the MMC infants underwent a revision operation in contrast to the control group of 40%. CONCLUSION: The presented shunt strategy showed improved revision free survival rates in infants with a MMC-related hydrocephalus in comparison to other etiologies of hydrocephalus in infants, which might relate to infection prophylaxis and high drainage resistance integrated in the shunt system.
11) 2016, May, Gebert A. F., Schulz M., Schwarz K. and Thomale U. W.: "Long-term survival rates of gravity-assisted, adjustable differential pressure valves in infants with hydrocephalus",
J Neurosurg Pediatr 17(5): 544-551,
Abstr.: OBJECTIVE The use of adjustable differential pressure valves with gravity-assisted units in shunt therapy of children with hydrocephalus was reported to be feasible and promising as a way to avoid chronic overdrainage. In this single-center study, the authors' experiences in infants, who have higher rates of shunt complications, are presented. METHODS All data were collected from a cohort of infants (93 patients [37 girls and 56 boys], less than 1 year of age [mean age 4.1 +/- 3.1 months]) who received their first adjustable pressure hydrocephalus shunt as either a primary or secondary implant between May 2007 and April 2012. Rates of valve and shunt failure were recorded for a total of 85 months until the end of the observation period in May 2014. RESULTS During a follow-up of 54.2 +/- 15.9 months (range 26-85 months), the Kaplan-Meier rate of shunt survival was 69.2% at 1 year and 34.1% at 85 months; the Kaplan-Meier rate of valve survival was 77.8% at 1 year and 56% at 85 months. Survival rates of the shunt were significantly inferior if the patients had previous shunt surgery. During follow-up, 44 valves were exchanged in cases of infection (n = 19), occlusion (n = 14), dysfunction of the adjustment unit (n = 10), or to change the gravitational unit (n = 1). CONCLUSIONS Although a higher shunt complication rate is observed in infant populations compared with older children, reasonable survival rates demonstrate the feasibility of using this sophisticated valve technology. The gravitational unit of this valve is well tolerated and its adjustability offers the flexible application of opening pressure in an unpredictable cohort of patients. This may adequately address overdrainage-related complications from early in treatment.
12) 2015, Aug, Xinxing L., Hongyu D. and Yunhui L.: "Using individualized opening pressure to determine the optimal setting of an adjustable proGAV shunt in treatment of hydrocephalus in infants",
Childs Nerv Syst 31(8): 1267-1271,
Abstr.: INTRODUCTION: The aim of the study was to describe the authors' experiences with the adjustable gravitational proGAV shunt system in treating infants' hydrocephalus. PATIENTS AND METHODS: The proGAV was implanted in 29 infants (11 boys and 18 girls, median age 9 months) with hydrocephalus of various origins between January 2010 and June 2014. The opening pressure was chosen based on the intraventricular pressure which was measured during operation, and a gravitational unit with a fixed opening pressure (15 cm H2O) was selected. RESULT: Regular clinical follow up ranged from 6 to 36 months, with a mean follow-up time of 15.7 +/- 7.9 months. Five of these patients (17.2%) underwent shunt revision because of malfunction, including two infections (6.9%), two shunt exposed (6.9%), and one proximal catheter occlusion (3.4%). For readjustment in 10 infants, the opening pressure was changed at least once during the follow-up period. CONCLUSION: The proGAV is efficacious in the treatment of hydrocephalus in infants. This individual selection of the opening pressures makes it probable that a better match of chosen opening pressure and actual hydraulic requirements of the patient might occur.
13) 2015, Apr, Suchorska B., Kunz M., Schniepp R., Jahn K., Goetz C., Tonn J. C. and Peraud A.: "Optimized surgical treatment for normal pressure hydrocephalus: comparison between gravitational and differential pressure valves",
Acta Neurochir (Wien) 157(4): 703-709,
Abstr.: OBJECTIVES: In idiopathic normal pressure hydrocephalus (NPH) ventriculoperitoneal (VP) shunt insertion is the method of choice to improve cardinal symptoms such as gait disturbance, urge incontinence and/or dementia. With reduced compliance, the brain of the elderly is prone for overdrainage complications. This was especially true with the use of differential pressure valve implantation. The present study compares clinical outcome and complication rates after VP shunt insertion with differential pressure valves in the early years and gravitational valves since 2005. METHODS: The authors reviewed patients treated at our institution for NPH since 1995. Differential pressure valves were solely used in the initial years, while the treatment regimen changed to gravitational valves in 2005. Clinical improvement/surgical success rates as well as complications were compared between the two groups. RESULTS: Eighty-nine patients were enrolled for the present study. Mean age at the time of surgery was 73.5 +/- 6.3 years. Male patients predominated with 73, compared with 16 female patients. Median follow-up time was 28 +/- 26 months. Date of last follow-up was 1st October 2013. Forty-nine patients received a gravitational valve, while 40 were treated with differential pressure valves. In the gravitational group a significant improvement was observed after shunt insertion for gait disorder, cognitive impairment and urge incontinence (p < 0.0001, resp. p = 0.004), while a significant change in the differential pressure group was only seen for gait disorder (p = 0.03) but not for cognition or urinary incontinency (p > 0.05). The risk of hygroma as a sign of shunt overdrainage requiring surgical intervention was significantly higher in the differential pressure group (5 versus 0 in the gravitational group). CONCLUSIONS: Patients with NPH treated with gravitational valves in the present cohort showed a more profound improvement in their initial symptoms, including gait disorder, cognitive impairment and urinary incontinency without the risk of overdrainage complications requiring surgical intervention when compared with patients who received differential pressure valves in previous years.
14) 2015, Oct, Kehler U., Kiefer M., Eymann R., Wagner W., Tschan C. A., Langer N., Rohde V., Ludwig H. C., Gliemroth J., Meier U., Lemcke J., Thomale U. W., Fritsch M., Krauss J. K., Mirzayan M. J., Schuhmann M. and Huthmann A.: "PROSAIKA: a prospective multicenter registry with the first programmable gravitational device for hydrocephalus shunting",
Clin Neurol Neurosurg 137: 132-136,
Abstr.: OBJECTIVE: Cerebrospinal fluid (CSF) overdrainage is a major problem in shunt therapy for hydrocephalus. The adjustable gravitational valve proSA allows for the first time a targeted compensation for overdrainage in the upright position without interfering with the differential pressure valve. To evaluate benefit, safety and reliability, the multicenter prospective registry PROSAIKA was conducted in 10 German neurosurgical centers. METHODS: Between March 2009 and July 2010, 120 hydrocephalic patients undergoing first time shunt implantation or shunt revision using proSA entered the study. 93 patients completed the 12 months follow-up. RESULTS: Hydrocephalus symptoms were improved in 86%, unchanged in 9% and deteriorated in 3%. In 51%, the proSA opening pressure was readjusted one or several times to treat suspected suboptimal shunt function, this resulted in clinical improvement in 55%, no change in 25%, and deterioration in 20% of these patients. The 1 year censored proSA shunt survival rate was 89%. Device related shunt failure was seen in two cases. CONCLUSIONS: This is the first clinical report on the implantation of the adjustable gravitational valve proSA with a follow-up of 12 months in a substantial number of patients. Irrespective of different hydrocephalus etiologies and indications for shunt surgery, the overall results after 12 months were very satisfying. The high frequency of valve readjustments underlines the fact that preoperative selection of the appropriate valve opening pressure is difficult. The low number of revisions and complications compared to other valves proves that proSA implantation adds no further risk; this valve is reliable, helpful and safe.
15) 2013, Mar, Thomale U. W., Gebert A. F., Haberl H. and Schulz M.: "Shunt survival rates by using the adjustable differential pressure valve combined with a gravitational unit (proGAV) in pediatric neurosurgery",
Childs Nerv Syst 29(3): 425-431,
Abstr.: OBJECTIVES: Overdrainage is a chronic complication in shunted pediatric patients with hydrocephalus. The use of adjustability of differential pressure (DP) valves in combination with antisiphoning devices may help to overcome this sequela and may diminish the rate of possible shunt failures. The purpose of this retrospective study is to report our experience on shunt survival and infection rate with an adjustable DP valve with integrated gravitational unit in pediatric hydrocephalus. METHODS: The proGAV consists of an adjustable differential pressure (DP) valve and a gravitational unit. During the time period of July 2004 and December 2009, a total of 237 adjustable gravitational valves were used in 203 children (age, 6.5 +/- 6.54; 0-27 years). In the follow-up period, valve and shunt failures as well as rate of infection were recorded. RESULTS: Within the average follow-up time of 21.9 +/- 10.3 months (range, 6-72 months), the valve survival rate was 83.8 %. The overall shunt survival rate including all necessary revisions was 64.3 %. Looking at the group of infants (<1 year of age) within the cohort, the valve survival rate was 77.3 % and the shunt survival rate was 60.9 %. The overall infection rate was 4.6 %. CONCLUSION: In a concept of avoiding chronic overdrainage by using the proGAV in hydrocephalic children, we observed a good rate of valve and shunt survival. Compared to previous reported series, we experienced the proGAV as a reliable tool for the treatment of pediatric hydrocephalus.
16) 2013, Aug, Lemcke J., Meier U., Muller C., Fritsch M. J., Kehler U., Langer N., Kiefer M., Eymann R., Schuhmann M. U., Speil A., Weber F., Remenez V., Rohde V., Ludwig H. C. and Stengel D.: "Safety and efficacy of gravitational shunt valves in patients with idiopathic normal pressure hydrocephalus: a pragmatic, randomised, open label, multicentre trial (SVASONA)",
J Neurol Neurosurg Psychiatry 84(8): 850-857,
Abstr.: OBJECTIVES: To investigate whether gravitational valves reduce the risk of overdrainage complications compared with programmable valves in ventriculoperitoneal (VP) shunt surgery for idiopathic normal pressure hydrocephalus (iNPH). BACKGROUND: Patients with iNPH may benefit from VP shunting but are prone to overdrainage complications during posture changes. Gravitational valves with tantalum balls are considered to reduce the risk of overdrainage but their clinical effectiveness is unclear. METHODS: We conducted a pragmatic, randomised, multicentre trial comparing gravitational with non-gravitational programmable valves in patients with iNPH eligible for VP shunting. The primary endpoint was any clinical or radiological sign (headache, nausea, vomiting, subdural effusion or slit ventricle) of overdrainage 6 months after randomisation. We also assessed disease specific instruments (Black and Kiefer Scale) and Physical and Mental Component Scores of the Short Form 12 (SF-12) generic health questionnaire. RESULTS: We enrolled 145 patients (mean (SD) age 71.9 (6.9) years), 137 of whom were available for endpoint analysis. After 6 months, 29 patients in the standard and five patients in the gravitational shunt group developed overdrainage (risk difference -36%, 95% CI -49% to -23%; p<0.001). This difference exceeded predetermined stopping rules and resulted in premature discontinuation of patient recruitment. Disease specific outcome scales did not differ between the groups although there was a significant advantage of the gravitational device in the SF-12 Mental Component Scores at the 6 and 12 month visits. CONCLUSIONS: Implanting a gravitational rather than another type of valve will avoid one additional overdrainage complication in about every third patient undergoing VP shunting for iNPH.
17) 2013, Nov, Gebert A. F., Schulz M., Haberl H. and Thomale U. W.: "Adjustments in gravitational valves for the treatment of childhood hydrocephalus-a retrospective survey",
Childs Nerv Syst 29(11): 2019-2025,
Abstr.: OBJECTIVE: Debatable disadvantages of preset differential pressure valves in treating pediatric hydrocephalus are the inability to treat over- and underdrainage after implantation without further surgery. This survey aims to retrospectively determine whether adjustments were performed and effectively used for the individual adaptation of CSF drainage from the shunted patients' and families' perspective. METHODS: In a series of 132 consecutive patients (59girls; 73boys, 0-29 years), families, caretakers, or the patients themselves were interviewed about their experiences after using the proGAV (Miethke-Aesculap, Germany) within a CSF-diverting shunt system. Thereby, the necessity and amounts of adjustments were evaluated. The subjective experiences of the adjustment process as well as the subsequent surgical interventions were documented with a follow-up period of 25.6 +/- 9 months. RESULTS: In 87.9 % of the cases, clinical symptoms improved subjectively after valve implantation. A total of 103 adjustments in 69 patients were performed. In 30 % of patients, more than one readjustment was done. As subjective experience, the adjustment process was described by 85 % of patients as painless or merely uncomfortable. Symptoms improved in 91 % in connection to a new pressure setting. During the entire follow-up period, 61 % of all patients remained free of surgery. CONCLUSION: The recently used adjustable valves provide good clinical results and seem to lead to satisfactory treatment from the perspective of the affected patients or caretakers. Although a mechanical manipulation of the skin is necessary, the mechanism of the integrated adjustment unit was mostly well tolerated and allows for a noninvasive and MRI stable treatment of over- and underdrainage.
18) 2013, Jul 4, Freimann F. B., Vajkoczy P. and Sprung C.: "Patients benefit from low-pressure settings enabled by gravitational valves in normal pressure hydrocephalus",
Clin Neurol Neurosurg 115(10): 1982-1986,
Abstr.: OBJECTIVE: The ability of siphon regulatory devices to improve overdrainage control despite low-pressure settings of the valve for the horizontal body position has been described previously. We aim to provide a systematic investigation on the ability of gravitational units as siphon regulatory devices to improve clinical outcome in shunt therapy. METHODS: We analyzed retrospectively postoperative complications, type and frequency of valve adjustments and the clinical outcome using Black's outcome scale at different time points of all iNPH patients operated in our center between January 2007 and December 2010. They had received either a proGAV(R) valve with an integrated gravitational unit, or a programmable Codman Hakim(R) valve without an integrated siphon regulatory device. RESULTS: The postoperative course of 55 proGAV(R) and 45 programmable Codman Hakim(R) patients was analyzed. The latest documented valve setting of the proGAV(R) group and Codman Hakim(R) group was median 50mm H2O and 120mm H2O, respectively. Overdrainage occurred among both groups in 20% of the patients, while surgical intervention for overdrainage-related complications was seen to be necessary only in 7% of the cases in the Codman Hakim(R) group. Clinical outcome differed in an increasing manner over the observation period (median 4 points after 3, 12 months and at final presentation in the proGAV(R); median 4 points after 3 and 12 months and 3 points at final presentation in Codman Hakim(R) group (p=0.001)). CONCLUSION: Adjustable and gravity-assisted valves like the proGAV(R) improve overdrainage control and enable thus low-pressure settings for the horizontal body position. We observed an improved and more sustainable functional outcome for iNPH patients with an adjustable and gravity-assisted valve compared to iNPH patients without an integrated siphon regulatory device.
19) 2017, Oct 27, Sundstrom N., Lagebrant M., Eklund A., Koskinen L. D. and Malm J.: "Subdural hematomas in 1846 patients with shunted idiopathic normal pressure hydrocephalus: treatment and long-term survival",
J Neurosurg: 1-8,
Abstr.: OBJECTIVE Subdural hematoma (SDH) is the most common serious adverse event in patients with shunts. Adjustable shunts are used with increasing frequency and make it possible to noninvasively treat postoperative SDH. The objective of this study was to describe the prevalence and treatment preferences of SDHs, based on fixed or adjustable shunt valves, in a national cohort of patients with shunted idiopathic normal pressure hydrocephalus (iNPH), as well as to evaluate the effect of SDH and treatment on long-term survival. METHODS Patients with iNPH who received a CSF shunt in Sweden from 2004 to 2015 were included in a prospective quality registry (n = 1846) and followed regarding SDH, its treatment, and mortality. The treatment of SDH was categorized into surgery, opening pressure adjustments, or no treatment. RESULTS During the study period, the proportion of adjustable shunts increased from 75% to 95%. Ten percent (n = 184) of the patients developed an SDH. In 103 patients, treatment was solely opening pressure adjustment. Surgical treatment was used in 66 cases (36%), and 15 (8%) received no treatment. In patients with fixed shunt valves, 90% (n = 17) of SDHs were treated surgically compared with 30% (n = 49) in patients with adjustable shunts (p < 0.001). There was no difference in long-term patient survival between the SDH and non-SDH groups or between different treatments. CONCLUSIONS SDH remains a common complication after shunt surgery, but adjustable shunts reduced the need for surgical interventions. SDH and treatment did not significantly affect survival in this patient group, thus the noninvasive treatment offered by adjustable shunts considerably reduces the level of severity for this common adverse event.
20) 2019, Aschoff A: "In-Depth View: Functional Characteristics of CSF Shunt Devices (Pros and Cons)",
In “Textbook of Pediatric Neurosurgery” (Editor: Di Rocco)